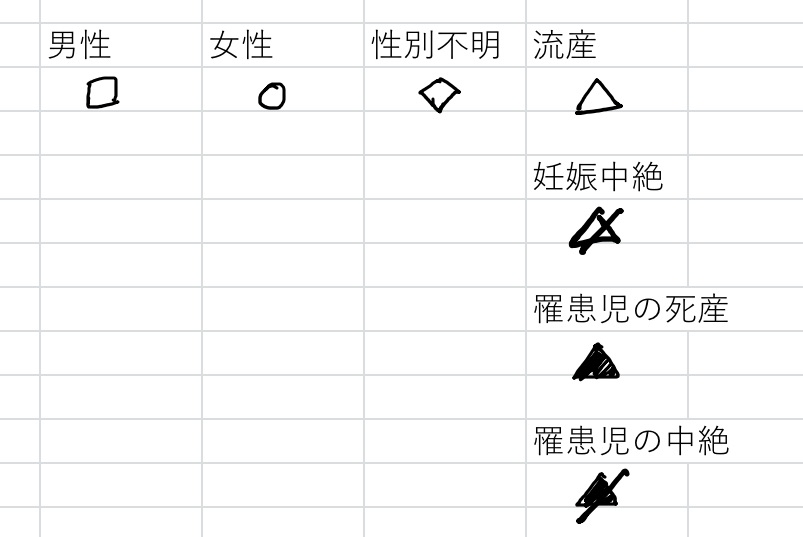
減数分裂はなぜ必要なのか?
ヒトの細胞の中は、常染色体として相同染色体(母由来と父由来の染色体が2本で1対)が22対とXXまたはXY染色体が入っており、計46本の染色体で成り立っています。これをそのままコピーしてしまうと、誕生する子の染色体数は精子の46本と卵子の46本を合わせて92本になってしまいます。したがって、生殖細胞は2回分裂することによって、細胞1個あたりの染色体数を23本 に半減させるのです。これを「減数分裂」と言います。
相同染色体は第一減数分裂で(同じ)染色体同士が対合(たいごう)した後に分離され、さらに第二減数分裂でも二価染色体が分離され、配偶子(卵子、精子)が作られます。
胎生期(母親のお腹にいる間)に胎児卵巣内での細胞の減数分裂は始まっており、第一減数分裂の前期で一旦停止します。思春期に排卵周期が開始されてから第一減数分裂が再開されます。女性は実に10数年減数分裂が停止していることになります。
 長腕同士で相同染色体、短腕同士で相同染色体。複製し(白色)長腕同士の相同染色体と(赤色)長腕同士の相同染色体が対合、いわばくっついているのを二価染色体と呼ぶ。よって短腕のものも含めると2つの二価染色体が成り立つ
長腕同士で相同染色体、短腕同士で相同染色体。複製し(白色)長腕同士の相同染色体と(赤色)長腕同士の相同染色体が対合、いわばくっついているのを二価染色体と呼ぶ。よって短腕のものも含めると2つの二価染色体が成り立つ
一方、精子形成においての第一・第二減数分裂は思春期以降に続いて行われます。
母体年齢が上昇すると、受精可能な卵子形成時の染色体不分離の頻度が増加する
生殖細胞のストック数は出生時に既に決定され、その後増えることはありません。女性が一生で排卵する卵子は400 〜500個とされています。受精できる卵子は排卵時に原則1つ作られるので、年齢を重ねるごとにその時排卵される卵子は減数分裂の停止期間が長くなっていきます。これが染色体の不分離を起こしやすくなり、ひいては高年妊娠でダウン(Down)症候群(21トリソミー)の発生率が高くなる理由となります。
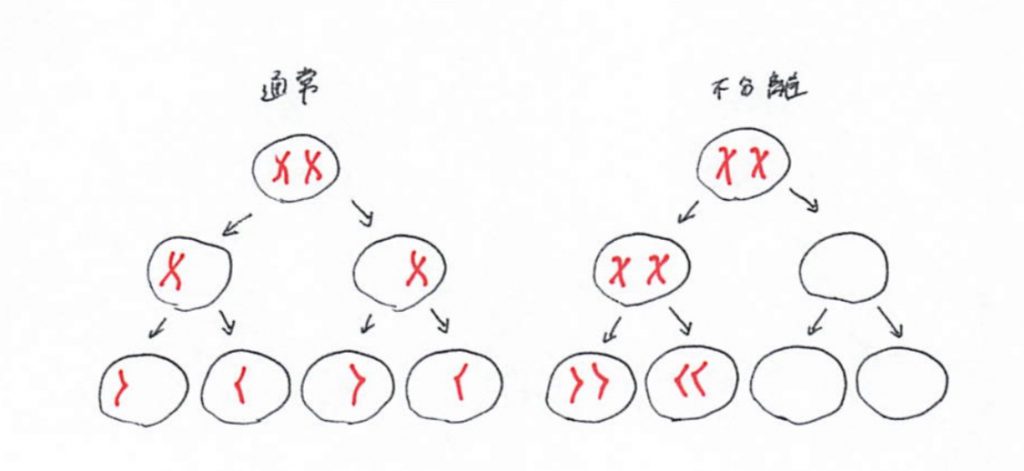 減数分裂は1つの母細胞から2回分裂して4つの娘細胞ができる。染色体は2倍体であり、数(n)として「2n」と表す。通常、減数分裂は2n(母細胞1つ)から→第1減数分裂でn:片親分(細胞自体が分裂するので細胞は2個)→第2減数分裂でn:片親分(さらに分裂するので細胞は4つ。DNA含有量は2コピーから1コピーとなる)
減数分裂は1つの母細胞から2回分裂して4つの娘細胞ができる。染色体は2倍体であり、数(n)として「2n」と表す。通常、減数分裂は2n(母細胞1つ)から→第1減数分裂でn:片親分(細胞自体が分裂するので細胞は2個)→第2減数分裂でn:片親分(さらに分裂するので細胞は4つ。DNA含有量は2コピーから1コピーとなる)
第一減数分裂での染色体の形成が、のちの配偶子形成に左右される
生殖細胞は通常、第一減数分裂で二価染色体を形成しますが、
ロバートソン転座保因者は第一減数分裂で三価染色体を形成し、その後の配偶子形成、そして受精で21トリソミーが起こる(隣接分離では不均衡型の配偶子を形成し、正常一倍体の配偶子と受精した場合に)可能性があります。
均衡型相互転座保因者の第一減数分裂では、転座に関わる染色体2本とそれらに対応する正常染色体2本の相同部位が対合して四価染色体を形成し、のちに不均衡型転座をもつ児が出生する可能性があります。
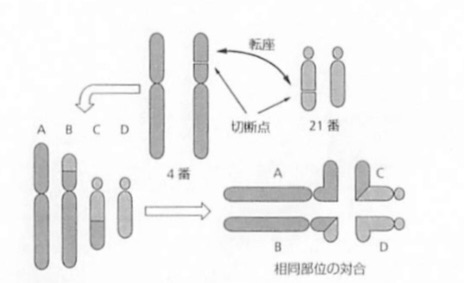 四価染色体の形成(出典:周産期遺伝カウンセリングマニュアル改訂4版. 中外医学社)
四価染色体の形成(出典:周産期遺伝カウンセリングマニュアル改訂4版. 中外医学社)
*均衡型相互転座の減数分裂、いわば四価染色体が分離する時、中でも遺伝子量がバランスよく分配されたもの(2:2の交互分離)であれば、児は保因者の片親と同じ均衡型相互転座を引き継いだ状態(表現型が親と同じ)となり得ます。
四価染色体がアンバランスに分配された、例えば3:1分離は全て不均衡型の配偶子となります。受精した場合先天異常を有します。
執筆 院長